Europij, simbol je Eu, atomsko število pa je 63. Kot tipičen član lantanoidov ima evropij običajno valenco +3, pogosta pa je tudi valenca kisika +2. Manj je spojin evropija z valenco +2. V primerjavi z drugimi težkimi kovinami evropij nima pomembnih bioloških učinkov in je relativno nestrupen. Večina uporab evropija uporablja učinek fosforescence evropskih spojin. evropij je eden najmanj zastopanih elementov v vesolju; v vesolju je le približno 5 × 10⁻⁶ % snovi je evropija.
Europij obstaja v monazitu
Odkritje evropija
Zgodba se začne konec 19. stoletja: takrat so odlični znanstveniki začeli sistematično zapolnjevati preostala prazna mesta v Mendelejevem periodnem sistemu z analizo atomskega emisijskega spektra. Z današnjega vidika to delo ni težko in ga lahko opravi že dodiplomski študent; takrat pa so imeli znanstveniki le instrumente z nizko natančnostjo in vzorce, ki jih je bilo težko prečistiti. Zato so v celotni zgodovini odkritja lantanida vsi "kvazi" odkritji nenehno podajali lažne trditve in se prepirali med seboj.
Leta 1885 je Sir William Crookes odkril prvi, a ne zelo jasen signal elementa 63: v vzorcu samarija je opazoval specifično rdečo spektralno črto (609 nm). Med letoma 1892 in 1893 je odkritelj galija, samarija in disprozija, Paul é mile LeCoq de Boisbaudran, potrdil ta pas in odkril še en zeleni pas (535 nm).
Nato je leta 1896 Eugène Anatole Demar potrpežljivo ločil samarijev oksid in potrdil odkritje novega redkozemeljskega elementa, ki se nahaja med samarijem in gadolinijem. Ta element je uspešno ločil leta 1901, s čimer je zaznamoval konec odkritja: »Upam, da bom ta novi element poimenoval evropij, s simbolom Eu in atomsko maso približno 151.«
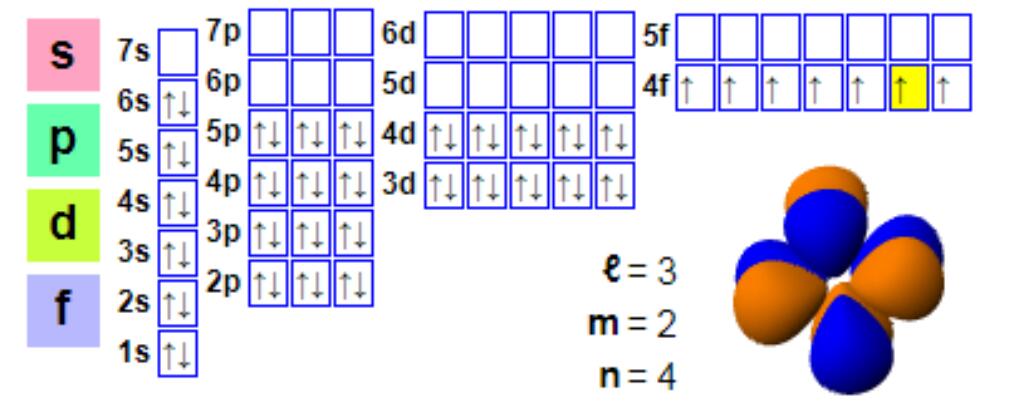
Elektronska konfiguracija
Elektronska konfiguracija:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p66s2 4f7
Čeprav je evropij običajno trivalenten, je nagnjen k tvorbi dvovalentnih spojin. Ta pojav se razlikuje od tvorbe spojin z +3 valenco pri večini lantanidov. Dvovalentni evropij ima elektronsko konfiguracijo 4f7, saj delno napolnjena f-lupina zagotavlja večjo stabilnost, evropij (II) in barij (II) pa sta si podobna. Dvovalentni evropij je blago redukcijsko sredstvo, ki na zraku oksidira in tvori spojino evropija (III). V anaerobnih pogojih, zlasti pri segrevanju, je dvovalentni evropij dovolj stabilen in se nagiba k vgradnji v kalcij in druge zemeljskoalkalijske minerale. Ta proces ionske izmenjave je osnova za "negativno anomalijo evropija", kar pomeni, da imajo številni lantanoidni minerali, kot je monazit, v primerjavi z obilico hondrita nizko vsebnost evropija. V primerjavi z monazitom bastnezit pogosto kaže manj negativnih anomalij evropija, zato je bastnezit tudi glavni vir evropija.
Europij je železovo siva kovina s tališčem 822 °C, vreliščem 1597 °C in gostoto 5,2434 g/cm³. Je najmanj gost, najmehkejši in najbolj hlapni element med redkozemeljskimi elementi. Europij je med redkozemeljskimi elementi najbolj aktivna kovina: pri sobni temperaturi na zraku takoj izgubi kovinski sijaj in se hitro oksidira v prah. Burno reagira s hladno vodo, pri čemer nastane vodikov plin. Europij lahko reagira z borom, ogljikom, žveplom, fosforjem, vodikom, dušikom itd.
Uporaba evropija
Europijev sulfat pod ultravijolično svetlobo oddaja rdečo fluorescenco
Georges Urbain, mladi izjemen kemik, je podedoval spektroskopski instrument Demarçaya in leta 1906 ugotovil, da vzorec itrijevega(III) oksida, dopiran z evropijem, oddaja zelo svetlo rdečo svetlobo. To je začetek dolge poti evropijevih fosforescentnih materialov – ki se niso uporabljali le za oddajanje rdeče, temveč tudi modre svetlobe, saj emisijski spekter Eu2+ spada v to območje.
Fosfor, sestavljen iz rdečih Eu3+, zelenih Tb3+ in modrih Eu2+ sevalnikov ali njihove kombinacije, lahko pretvori ultravijolično svetlobo v vidno svetlobo. Ti materiali igrajo pomembno vlogo v različnih instrumentih po vsem svetu: zaslonih za ojačanje rentgenskih žarkov, katodnih ceveh ali plazemskih zaslonih, pa tudi v novejših energetsko varčnih fluorescenčnih sijalkah in svetlečih diodah.
Fluorescenčni učinek trivalentnega evropija lahko senzibilizirajo tudi organske aromatske molekule, takšni kompleksi pa se lahko uporabljajo v različnih situacijah, ki zahtevajo visoko občutljivost, kot so črnila proti ponarejanju in črtne kode.
Od osemdesetih let prejšnjega stoletja ima evropij vodilno vlogo v visoko občutljivih biofarmacevtskih analizah z uporabo časovno ločljive metode hladne fluorescence. V večini bolnišnic in medicinskih laboratorijev je takšna analiza postala rutinska. V raziskavah na področju znanosti o življenju, vključno z biološkim slikanjem, so fluorescenčne biološke sonde iz evropija in drugih lantanidov vseprisotne. Na srečo je en kilogram evropija dovolj za podporo približno ene milijarde analiz – potem ko je kitajska vlada nedavno omejila izvoz redkih zemelj, industrializiranim državam, ki jih je prestrašilo pomanjkanje zalog redkih zemelj, ni treba skrbeti za podobne grožnje pri takšnih aplikacijah.
Europijev oksid se uporablja kot fosfor za stimulirano emisijo v novem rentgenskem medicinskem diagnostičnem sistemu. Europijev oksid se lahko uporablja tudi za izdelavo barvnih leč in optoelektronskih filtrov, za magnetne naprave za shranjevanje mehurčkov ter v kontrolnih materialih, zaščitnih materialih in strukturnih materialih atomskih reaktorjev. Ker lahko njegovi atomi absorbirajo več nevtronov kot kateri koli drug element, se pogosto uporablja kot material za absorpcijo nevtronov v atomskih reaktorjih.
V današnjem hitro rastočem svetu bi lahko nedavno odkrita uporaba evropija močno vplivala na kmetijstvo. Znanstveniki so ugotovili, da lahko plastika, dopirana z dvovalentnim evropijem in enovalentnim bakrom, učinkovito pretvori ultravijolični del sončne svetlobe v vidno svetlobo. Ta postopek je precej zelen (gre za komplementarne barve rdeče). Uporaba te vrste plastike za gradnjo rastlinjaka lahko rastlinam omogoči, da absorbirajo več vidne svetlobe in povečajo pridelek za približno 10 %.
Europij se lahko uporablja tudi v kvantnih pomnilniških čipih, ki lahko zanesljivo shranjujejo informacije več dni hkrati. Ti omogočajo shranjevanje občutljivih kvantnih podatkov v napravi, podobni trdemu disku, in njihovo pošiljanje po vsej državi.
Čas objave: 27. junij 2023